
국산 코로나19 백신 첫 3상 돌입
김향미·노도현 기자 sokhm@kyunghyang.com / 2021.08.10. 21:18
SK바이오 ‘재조합 백신’
이르면 내년 상반기 허가
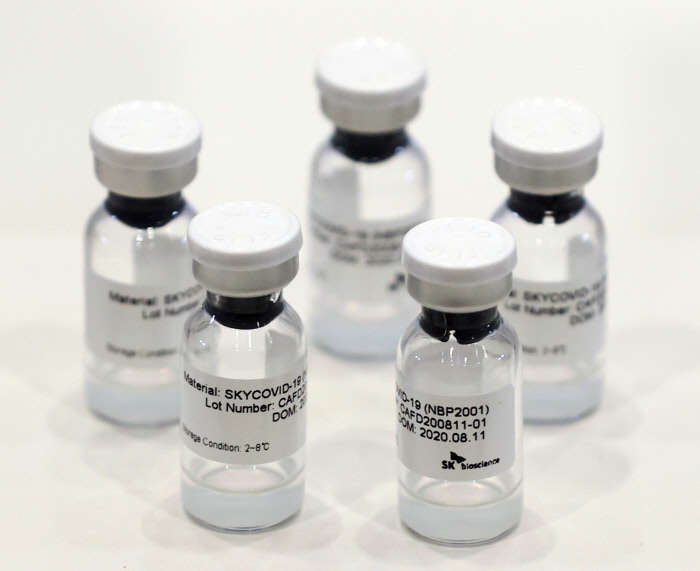
국내 기업이 개발 중인 코로나19 백신 후보군이 처음으로 임상시험의 최종 단계인 3상 시험에 진입했다. 이르면 내년 상반기 중 상용화될 것으로 전망된다.
식품의약품안전처는 SK바이오사이언스의 코로나19 백신 ‘GBP510’의 3상 임상시험 계획에 대해 안전성과 과학적 타당성을 검증해 10일 승인했다고 밝혔다. 김강립 식약처장은 이날 브리핑에서 “국내 백신 자급화를 위한 첫걸음”이라며 내년 1분기 중 업체 측이 해당 백신의 품목 허가 신청을 할 것으로 전망된다고 밝혔다.
GBP510은 유전자 재조합 기술을 이용해 만든 코로나19 바이러스의 표면항원 단백질을 주입해 면역반응을 유도하는 ‘재조합 백신’이다. 임상 3상은 이미 허가가 난 백신과의 비교로 효과를 입증하는 비교임상 방식으로, 안전성과 면역원성을 평가한다.
SK바이오사이언스 측은 같은 재조합 백신군인 노바백스 백신 승인이 나지 않은 상황에서 바이러스벡터 백신인 아스트라제네카(AZ) 백신을 대조 백신으로 선정했다. AZ사와는 협의를 마쳤다. 식약처는 대조 백신의 플랫폼이 달라도 비교임상에는 문제가 없다고 밝혔다.
먼저 코로나19 백신 비교임상(3상)을 시작한 프랑스 발네바사도 다른 플랫폼 백신을 대조 백신으로 삼았다. 홍기종 대한백신학회 편집위원장은 “다만 플랫폼이 다르기 때문에 임상시험 설계도 더 정교하게 짜야 하고, 승인 기준도 높아질 수 있어 임상 진행에 부담이 되는 부분은 있을 것”이라고 말했다.
전체 시험 대상자는 18세 이상 3990명이며 시험 백신은 3000명, 대조 백신은 990명에게 0.5㎖씩 4주 간격으로 2회 접종한다. 식약처 전문가 자문 결과에 따라 AZ 백신의 부작용으로 알려진 혈전증이나 면역혈소판감소증 등을 앓는 자가면역질환자는 제외된다.
이번 임상 3상은 국내와 동남아시아, 동유럽 등에서 동시에 수행될 예정이다. 국내는 고령층 접종률이 높아 참여자 모집이 어려울 수 있는데, 정부가 태스크포스(TF)를 가동해 지원에 나선다.
김향미·노도현 기자 sokhm@kyunghyang.com
-------
이제 한국도 백신을 내놓게 됬다 참으로 다행한일
국내 기업이 개발 중인 코로나19 백신 후보군이 처음으로 임상시험의 최종 단계인 3상 시험에 진입하여
이르면 내년 상반기 중 상용화될 것으로 전망된다는 아주 반가운 뉴스
제발 그렇게 되기를 바란다
'이슈와 정치' 카테고리의 다른 글
| 탈레반 "전쟁 끝났다" 선언..'필사의 탈출' 공항선 발포까지 (0) | 2021.08.16 |
|---|---|
| 정경심 ‘자녀 입시비리·사모펀드 의혹’ 항소심 결과는 (0) | 2021.08.14 |
| 9개월만에 카메라 앞에 선 전두환..그가 손을 흔들어 보인 이유는? (0) | 2021.08.10 |
| "대역 아냐? 완전 딴사람"..전두환, 몇 달 새 급격히 달라진 모습 (0) | 2021.08.10 |
| '지사찬스' 공방 격화..이재명 "차라리 경선포기" (0) | 2021.08.07 |



